В современном мире из металлов самых разных видов производится большое количество продукции. Металлические материалы присутствуют в разных отраслях промышленности в виде станков и машин, инструментов. Очень важно при производстве какой –либо продукции сделать так, чтобы металлы как можно меньше покрывались ржавчиной или были устойчивы к ее появлению.
- Процесс коррозии
- Характеристики коррозии
- Типы коррозии
- Таблица. Виды электрохимической коррозии
- Ингибиторы коррозии
- Коррозия на авто
- Методы защиты металлов от коррозии
- Все способы защиты от коррозии металла, их плюсы и минусы
- Способы антикоррозийной защиты
- Первая
- Вторая
- Катодная защита
- Протекторная защита
- Поляризация анодная
- Создание защитной пленки
- Прокладка металлоконструкций в защитных «желобах»
- Фосфатирование
- Покрытие более устойчивыми материалами
- Пассивация
- Снижение агрессивности среды
- Обработка ядохимикатами
- Легирование
- Как защитить металлические изделия от коррозии?
- Основные виды коррозионных процессов
- Методы повышения сопротивляемости
- Снижение агрессивности внешней среды и электрохимическая защита
- Пленочная защита
- Коррозия металлов и методы защиты от коррозии
- Cпособы защиты металла от коррозии: основные методы и их особенности
- Антикоррозионная защита — зачем она нужна
- Защита изделий из металла от коррозии
- Борьба с коррозией при помощи органических покрытий
- Обработка неметаллическими неорганическими покрытиями
- Фосфатные пленки
- Оксидные пленки
- Дополнительные способы
- Заключение
Процесс коррозии
Характеристики коррозии
Коррозия в простонародии больше известная под названием ржавчина. Она представляет собой процесс самопроизвольного образования на металлической поверхности налета в результате влияния окружающей среды. Ржавчина обычно имеет темно-коричневый оттенок, который портит внешние качества изделия из того или иного металла.
Коррозия металла сегодня встречается достаточно часто. Причиной ее появления является то, что некоторые виды металлических материалов являются неустойчивыми к температурным перепадам и изменениям влажности. Изделиям из металлов достаточно часто приходится контактировать с различными веществами. Они могут влиять на них по-разному. В результате образуется коррозия различных видов.
В результате конструкция, которая из него создана, приходит в негодность.
Коррозии подвергаются не только металлы, но и другие материалы. Сегодня довольно часто встречаются случаи, когда она появляется на пластмассе. Образование ржавчины присуще и бетонным изделиям.
Скорость коррозии зависит от размера температуры. С повышением температуры на каждые сто градусов появление ржавчины становится быстрее.
Типы коррозии
В современном мире представлено большое количество видов такого процесса, как образование ржавчины на поверхности материалов отдельных видов.
Виды коррозии сегодня встречаются следующие:
- Электрохимическая коррозия. Данный вид образования коррозии характеризуется тем, что на поверхности металлов появляются гальванические элементы, которые вызывают появление ржавчины. Для появления данного типа коррозии необходимо наличие электролита. В его роли чаще всего выступает вода. При соприкосновении с конденсатом или водой электроды или другие элементы металла меняют свой оксилительно-восстановительный потенциал.
- Водородная коррозия. При данном виде коррозии отмечается водородная деполяризация. При этом водород восстанавливается.
- Кислородная коррозия. Бывают ситуации, когда водород в щелочной среде не имеет возможности выделяться. В результате выделяется кислород, который приводит к появлению налета ржавчины на металлической поверхности.
- Химическая коррозия. При данном виде коррозии поверхность металла соприкасается со средой, которая провоцирует появления ржавчины.
Таблица. Виды электрохимической коррозии
№ ппВид электрохимической коррозииСпособ прокладки трубопровода (вид оборудования)Дополнительные коррозионные факторы
| 1. | Атмосферная коррозия | Наружные поверхности трубопроводов наземной и канальной прокладки (при уровне подтопления и заиливания канала, не достигающим изоляционных конструкций). Поверхности различных металлоконструкций и оборудования, не контактирующие с водой и грунтом. | Внутренние напряжения в металле трубопровода и металлоконструкций, ударно-механическое воздействие капели с перекрытий. Характерные коррозионные повреждения: равномерная коррозия, в местах капели возможна коррозия пятнами. |
| 2. | Подземная коррозия | Наружные поверхности трубопроводов бесканальной прокладки (при нарушении целостности изоляции), канальной прокладки (периодическое подтопление и заиливание канала, сопровождающееся увлажнением тепловой изоляции). | Внутренние напряжения в металле, коррозия внешним постоянным и переменным током, воздействие капели. Характерные коррозионные повреждения: неравномерная коррозия, коррозия пятнами, при воздействии блуждающих токов возможны сквозные поражения стенки трубопровода. |
| 3. | Подводная коррозия | Наружные поверхности трубопроводов канальной прокладки. (Постоянное подтопление канала при отсутствии тепловой изоляции на трубопроводе). Внутренние поверхности трубопроводов и оборудования химводоподготовки (деаэраторы, фильтры и т.п.) | Внутренние напряжения в металле, коррозия внешним постоянным и переменным током. При неполном погружении трубопровода возможна коррозия по ватерлинии. Характерные коррозионные повреждения: неравномерная коррозия, при воздействии блуждающих токов возможны сквозные поражения стенки трубопровода, язвенные поражения в районе ватерлинии. На трубопроводах горячего водоснабжения возможно протекание процесса микробиологической коррозии железобактериями. Характерные коррозионные повреждения: язвенная коррозия (для внутренних поверхностей трубопроводов), точечная коррозия, неравномерная коррозия. |
Ингибиторы коррозии
Ингибитор коррозии представляют собой химические соединения, которые используются для блокирования или задержания процесса образования ржавчины. Ели они есть в агрессивной среде, что процесс образования коррозии на металлических поверхностях сократится в разы.
Ингибиторы образуют на поверхности металлов тонкую защитную пленку, которая не дает проникать в поры металлов воздуху и жидкостям, которые могут нарушить их целостность. Они являются одним из самых эффективных методов борьбы с образованием ржавчины.
Коррозия на авто
Многие современные автомобилисты сталкиваются с тем, что на автомобилях появляется со временем ржавчина. Чаще всего страдает от этого кузов авто. Коррозия автомобиля относится к разряду часто встречающихся ситуаций. Она появляется на тех деталях, которые не сделаны из нержавеющей стали.
Сегодня есть специальные средства, которые предотвращают появление ржавчины на деталях авто. Они представлены различными составами, которые наносятся на поверхность перед покраской.
Методы защиты металлов от коррозии
Коррозия каждый приводит к тому, что появляется большое количество убытков. Они исчисляются миллионами. Ущерб наносится не потому, что коррозия уничтожает металлы, а потому что в результате этого процесса портятся вещи из металлических материалов.
В мире применяется большое количество оборудования, которое в большинстве своем сделано из металлической основы. Его стоимость является достаточно высокой. После выхода из строя оборудования не каждая организации имеет возможность приобрести еще одно такого же уровня.
Именно поэтому так необходима защита от коррозии.
В современном мире очень важно правильно подобрать средства для борьбы с появлением ржавчины на металлических изделиях. Необходимо перед нанесением краски тщательно подготовить металлическую поверхность.
От этого зависит восемьдесят процентов противостояния образованию коррозии. Лакокрасочные материалы, которые наносятся в последующем, обеспечивают лишь двадцати процентную защиту.
Сегодня для обработки металлических поверхностей можно использовать специальные преобразователи ржавчины, которые выполняют роль и защиты и грунтовки.
Источник:
Все способы защиты от коррозии металла, их плюсы и минусы

Под воздействием внешних факторов (жидкости, газы, агрессивные химические соединения) разрушаются любые материалы. Не являются исключением и металлы. Коррозийные процессы нейтрализовать полностью невозможно, но вот снизить их интенсивность, повысив тем самым эксплуатационный срок металлоконструкций или иных, в состав которых входит «железо», вполне возможно.
Способы антикоррозийной защиты
Все способы защиты от коррозии можно условно классифицировать как методики, которые применимы или до начала эксплуатации образца (группа 1), или уже после его ввода в строй (группа 2).
Первая
- Повышение сопротивляемости «химическому» воздействию.
- Исключение прямого контакта с агрессивными веществами (изоляция поверхностная).
Вторая
- Снижение степени агрессивности окружающей среды (в зависимости от условий эксплуатации).
- Использование ЭМ полей (к примеру, «наложение» внешних эл/токов, регулирование их плотности и ряд других методик).
Применение того или иного способа защиты определяется индивидуально для каждой конструкции и зависит от нескольких факторов:
- вид металла;
- условия его эксплуатации;
- сложность проведения антикоррозийных мероприятий;
- производственные возможности;
- экономическая целесообразность.
В свою очередь, все методики подразделяются на активные (подразумевающие постоянное «воздействие» на материал), пассивные (которые можно охарактеризовать как многоразового применения) и технологические (использующиеся на этапе изготовления образцов).
Катодная защита
Целесообразно использовать, если среда, с которой контактирует металл – электропроводящая. На материал подается (систематически или постоянно) большой «минусовой» потенциал, который делает в принципе невозможным его окисление.
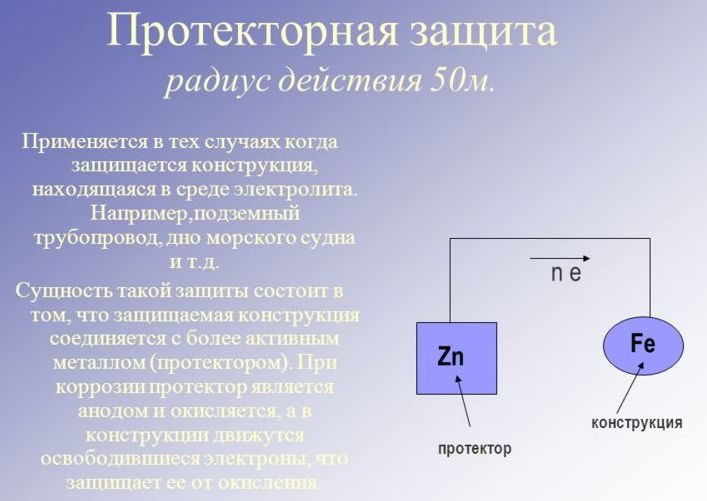
Протекторная защита
Заключается в катодной поляризации. Образец связывается контактом с материалом, который более подвержен окислению в данной токопроводящей среде (протектором). По сути, он является своего рода «громоотводом», принимая на себя весь «негатив», который создают агрессивные вещества. Но такой протектор нуждается в периодической замене на новый.
Поляризация анодная
Применяется крайне редко и заключается в поддержании «инертности» материала по отношению к внешним воздействиям.
Создание защитной пленки
Одна из самых распространенных и малозатратных методик борьбы с коррозией. Для создания поверхностного слоя используются вещества, которые должны соответствовать следующим основным требованиям – быть инертными по отношению к агрессивным хим/соединениям, не проводить эл/ток и обладать повышенной адгезией (хорошо скрепляться с основой).
Все используемые вещества в момент обработки металлов находятся в жидком или «аэрозольном» состоянии, от чего зависит и способ их нанесения – окраска или напыление. Для этого применяются лакокрасочные составы, различные мастики и полимеры.
Прокладка металлоконструкций в защитных «желобах»
Это характерно для разного вида трубопроводов и коммуникаций инженерных систем. В данном случае роль изолятора играет воздушная «прослойка» между внутренними стенками канала и поверхностью металла.
Фосфатирование
Металлы подвергаются обработке специальными средствами (окислителями). Они вступают с основой в реакцию, в результате чего на ее поверхности происходит отложение малорастворимых хим/соединений. Довольно эффективный способ защиты от влаги.
Покрытие более устойчивыми материалами
Примерами использования такой методики служат часто встречающиеся в быту изделия с хромировкой (о хромировании читайте здесь), с серебрением, «оцинковкой» и тому подобное.
Как вариант – защита керамикой, стеклом, покрытие бетоном, цементными растворами (обмазка) и так далее.
Пассивация
Смысл заключается в том, чтобы резко снизить химическую активность металла. Для этого производится обработка его поверхности соответствующими спецреактивами.
Снижение агрессивности среды
- Использование веществ, которые снижают интенсивность коррозийных процессов (ингибиторов).
- Осушка воздуха.
- Его хим/очистка (от вредных примесей) и ряд других методик, которые могут применяться и в быту.
- Гидрофобизация почвы (засыпки, введение в нее спецвеществ) с целью снижения агрессивности грунта.
Обработка ядохимикатами
Используется в случаях, когда есть вероятность развития так называемой «биокоррозии».
Легирование
Самый известный способ. Смысл в том, чтобы на основе металла создать сплав, инертный по отношению к агрессивным воздействиям. Но реализуется только в промышленных масштабах.
Как следует из приведенной информации, не все методики антикоррозийной защиты можно применять в быту. В этом плане возможности «частника» существенно ограничены.
Источник:
Как защитить металлические изделия от коррозии?

Коррозия оказывает разрушительное действие на изделия из металла и сплавы. При взаимодействии с окружающей средой металлические изделия покрываются пятнами в виде ржавчины. Чем более активный металл, тем он сильнее подвержен коррозии.
Коррозия оказывает разрушительное действие на автомобили, суда, коммуникации и другие металлические изделия, что может привести к утечке нефти, газа и другим негативным последствиям. Она отрицательно влияет на здоровье человека, а продукты окисления загрязняют окружающую среду.
Недопустима коррозия в авиационной, химической и атомной промышленности. Порой затраты на ремонт металлических изделий превышают стоимость материала, который был израсходован на их изготовление.
Основные виды коррозионных процессов
Виды коррозии металлов можно разделить по следующим признакам: характеру разрушения, коррозионной среде и механизму действия.
Исходя из характера разрушений, коррозия может быть:
- сплошной. При этом она может быть равномерной и неравномерной. При равномерной разрушается вся поверхность изделия. При неравномерной появляются пятна и точечные углубления;
- межкристаллитной. В этом случае она проникает вглубь изделия по границам зерен металла;
- транскристаллитной, при этом металл рассекается трещиной через зерно;
- избирательной. Происходит разрушение одной из составляющих сплава. Например, в латуни может разрушаться цинк.
- подповерхностной. Начинается на поверхности и постепенно проникает в верхние слои металла.
Существуют следующие виды коррозионной среды:
- атмосфера;
- газ;
- почва;
- жидкость (щелочь, кислота или солевые растворы).
Механизм действия разделяет коррозию на химическую и электрохимическую.
Химической коррозией называется процесс, при котором происходит самопроизвольное разрушение металлов. Он происходит при взаимодействии металлических изделий с активно-коррозионной средой, чаще всего газовой. Эти процессы сопровождаются высокими температурами.
В результате происходит одновременное окисление металла и восстановление коррозионной среды. Химическая коррозия происходит также при взаимодействии с органическими жидкостями, например, с нефтепродуктами, спиртом и др.
Электрохимическая коррозия возникает в электролитах, например, в водных растворах. Электрохимическая реакция вызывает электрический ток, который способствует разрушению металла. В этом случае происходят как химические процессы, при которых происходит отдача электронов, так и электрические, при которых движутся электроны.
Разнородность строения металла приводит к тому, что при электрохимической коррозии образуются по законам гальваники катодно-анодные пары. Если металлические изделия отличаются друг от друга химическим составом, то на поверхности металлических изделий образуется слой ржавчины.
Эта коррозия чаще всего является причиной разрушения металлов. Ниже приведены рисунки, на которых изображен механизм действия электрохимической коррозии.
Во внешней среде наиболее активно на металлические изделия действует кислород, повышенная влажность, оксиды серы, азота, углекислый газ, грунтовые воды. Соленая вода ускоряет процесс окисления, поэтому морские суда ржавеют быстрее, чем речные.
Остановить этот природный процесс невозможно, остается только найти способы защиты от коррозии. Правда, избавиться полностью от коррозионного процесса невозможно, но эти способы помогают замедлить сам процесс.
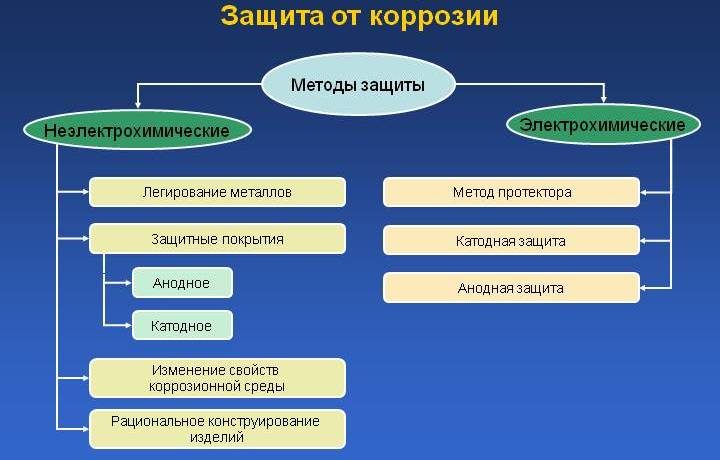
Для защиты металлов от коррозии существуют следующие методы:
- повышение сопротивляемости металлов за счет увеличения химического состава;
- изоляция металлических покрытий от агрессивного воздействия окружающей среды;
- снижение агрессивности среды, в которой происходит эксплуатация металлических изделий;
- электрохимические, которые, благодаря законам гальваники, снижают коррозионные процессы.
Эти методы можно разделить на две большие группы. Первые два метода применяются до того, как металлические изделия будут эксплуатироваться, то есть на стадии их производства. При этом выбираются определенные конструкционные материалы для производства изделия, наносятся различные гальванические и защитные покрытия.
Последние два метода применяются при эксплуатации металлических изделий. При этом для защиты пропускается ток через изделие, снижается агрессивность среды путем добавления различных ингибиторов, таким образом, до эксплуатации само изделие предварительно никак не обрабатывается.
Методы повышения сопротивляемости
Эти методы защиты основаны на создании сплавов, которые обладают антикоррозионными свойствами. К металлу добавляются компоненты, повышающие его коррозионную стойкость. Примером может служить легирование стали хромом.
Метод применяется при изготовлении стали. В результате получаются хромистые нержавеющие стали, которые устойчивы к коррозии. Повышают антикоррозионные характеристики сталей добавкой никеля, меди и кобальта.
На этих поверхностях не появляется ржавчина, но коррозия присутствует. Замедляется коррозия благодаря тому, что к восьми атомам железа добавляется один атом легирующей добавки, а это упорядочивает расположение атомов в кристаллической решетке твердого раствора, что и препятствует коррозии.
Коррозионную устойчивость можно повысить, удалив из металлов или сплавов примеси, которые ускоряют коррозию. Например, железо удаляют из сплавов магния или алюминия, серу из сплавов железа и т.д.
Снижение агрессивности внешней среды и электрохимическая защита
Снижение агрессивности внешней среды достигается путем удаления из нее веществ, которые являются деполяризаторами, или путем изоляции металлов от деполяризатора. Удаление кислорода из среды называется раскислением.
Для замедления коррозионного процесса в окружающую среду вводятся специальные вещества – ингибиторы. Они могут быть как органическими, так и неорганическими. Молекулы ингибиторов поглощаются поверхностью металла и, тем самым, способствуют резкому снижению скорости растворения металла и препятствуют протеканию электродных процессов.
В зависимости от сдвига потенциала электрохимическая защита может быть катодной и анодной. Эти способы применяют для защиты буровых платформ, сварных металлических оснований, трубопроводов, проходящих под землей, а также защищают подводные части морских судов.
Пленочная защита
Для того чтобы защитить металлические изделия от коррозии, можно нанести защитное покрытие. В качестве покрытия можно использовать лаки, краски, эмали, пластмассы и др.
Лакокрасочные покрытия легко наносятся, недорогие по стоимости, обладают водоотталкивающими свойствами, не вступают в химическую реакцию с металлом, хорошо заполняют поры и трещины. Они служат для защиты металлов от компонентов внешней среды, вызывающих коррозионные процессы.
Часто под лакокрасочное покрытие наносится грунтовка, проходя через которую, вода растворяет некоторые пигменты и становится не такой корррозионноактивной. Вместо грунтовки может проводится фосфатирование поверхности. Они наносятся кистью или распылителем. Для стальных изделий большинство таких препаратов состоит из смесей фосфатов марганца и железа.
Защитить металлическое изделие можно путем нанесения слоя металла, который более коррозионностойкий. В этом случае коррозия разрушает само покрытие. Такими металлами является хром, никель, цинк. Например, железо покрывается хромом.
Они служат для механической защиты основного металла. Если такое покрытие нарушается, антикоррозионная защита перестает действовать. Кроме того, при этом ускоряется коррозионный процесс.
Примером такого покрытия является покрытие железа оловом. Сравнивая эффективность анодного и катодного покрытия, лучше использовать анодное, так как оно действует даже при нарушении целостности покрытия.
Существуют различные способы получения металлических покрытий. При горячем способе покрытие получается путем опускания изделия в горячий металл.
Если изделие покрывается оловом, этот процесс называется лужением, если цинком – оцинкованием. Покрытие может наносится гальваническим методом путем осаждения на изделии солей из электролита.
При использовании метода напыления распыляется плазменная струя расплавленного металла и наносится на поверхность, которую надо защитить. Для распыления используются металлизаторы.
При плакировании осуществляется совместная горячая прокатка основного и защитного металла. Металлы сцепляются между собой благодаря диффузии.
Источник:
Коррозия металлов и методы защиты от коррозии
Коррозия химическое и (или) электрохимическое взаимодействие между металлическим материалом и окружающей средой, вызывающее изменение его свойств, что в большинстве случаев приводит к нарушению его функций.
По механизму разделится на химическую и электрохимическую.
Химическая коррозия – взаимодействие металла с коррозионной средой, при котором окисление металла и восстановление окислительного компонента среды протекает в одном акте при их непосредственном контакте.
Примеры: взаимодействие металлов с сухими газами при высоких t (газовая коррозия) и разрушение металлов в растворах неэлектролитов. Наиболее распространенный процесс газовой коррозии металлов –окислениe металлов O 2
Электрохимическая коррозия – взаимодействие Ме с коррозионной средой, при котором ионизация атомов металла и восстановление окислительного компонента среды протекает не в одном и том же акте, а в виде пространственно разделенных реакций, причем скорость этих реакций зависит от потенциала электрода. Электрохимическая коррозия обычно наблюдается в растворах электролитов.
По условиям протекания различают насколько видов коррозии: • газовая; • атмосферная; • жидкостная; • подземная; • биокоррозия; • коррозия при трении; • щелевая коррозия; • коррозия под механическим напряжением и др.
По характеру разрушения различают:
На поверхности металла одновременно (сопряженно) протекают два процесса: • анодный процесс ионизации (окисления) металла: • катодный процесс восстановления окислительного компонента среды: Ox и Red окисленная и восстановленная форма окислительного компонента среды. Электроны, освобождающиеся при окислении металла на одних участках его поверхности, потребляются при восстановлении окислителя на других участках.
Коррозия Zn с примесями Cu в кислой среде Анодные участки (Zn) Катодные участки (Cu)
Причиной коррозии металлов является их термодинамическая неустойчивость. Самопроизвольный процесс возможен, если он сопровождается убылью изобарно изотермического потенциала ( G). Это возможно, если равновесный потенциал металла отрицательнее равновесного потенциала реакции восстановления окислительного компонента среды.
При коррозии металлов в кислых растворах электролитов в качестве окислителя выступают ионы водорода водородная деполяризация
В нейтральных и щелочных электролитах окислителем может служить растворенный кислородная деполяризация
Возможны процессы и с металлической деполяризацией, когда в качестве деполяризатора выступают ионы : Например, при коррозии железа в растворе Cu. SO 4. Катодный процесс: Анодный процесс:
Количественные характеристики Скорость коррозии J= (m 0 m 1)/t. S, г/м 2 час Коэффициент торможения (для ингибиторной защиты) K= io/iи Степень защиты Z=(K 1)/K, %
Защита (Некоторые способы) Электрохимическая защита [катодная(внешним током и протекторная) и анодная] Покрытиями (металлические: катодные и анодные, неметаллические: органические и неорганические) Ингибиторами Обработка среды Комбинированные
Защита от коррозии осуществляется путем воздействия на М (объемное и поверхностное легирование), на среду (снижение концентрации окислителей и других агрессивных агентов или введение ингибиторов, в том числе пассиваторов), и на границу раздела металл-среда (нанесение покрытий и электрохимическая защита). Наиболее предпочтительно использование комбинированных методов, например, сочетание электрохимической защиты с покрытиями или ингибиторами, покрытий с ингибиторами и др.
Электрохимическая защита Она заключается в изменении Е металла, бывает катодной и анодной и осуществляется от внешнего источника тока (электрозащита) или путем контакта с металлом протектором (протекторная защита).
Анодная защита В её основе лежит явление пассивации М, эффективность равна: Эаз=[(j iпп)/j]∙ 100% (5) Анодная защита возможна только для анодно пассивирующихся М и осуществляется при помощи потенциостата (электрозащита) либо путем электрического контакта с катодным протектором (более эффективным катодом). Возможна анодная защита импульсным током iа>iп, если рост iа в пассивной области обусловлен выделением O 2 или другого OX, но не растворением М.
Покрытия защищают поверхность металла от коррозии путем ее изоляции от агрессивной среды, а также за счет торможения диффузии и электродных реакций.
Для этого покрытия должны обладать протекторным эффектом, коррозионной стойкостью и долговечностью, хорошей адгезией к подложке, сплошностью и беспористостью, сочетаться с другими средствами защиты и пр.
В зависимости от конкретных условий необходимо преобладание тех или иных факторов.
классификация а) по типу материала: металлические (металлы и сплавы); неметаллические: органические, (лакокрасочные, пластмассовые, гумировочные), неорганические (силикатные, оксидные, фосфатные) и комбинированные или композиционные; б) по деформационным свойствам (упругие, упругоэластичные, пластичные); в) по химической стойкости (химстойкие, относительно стойкие, нестойкие);
г) по теплостойкости (для диапазонов температур 50 70°, 70 100°, 100 150°, свыше 200°c); д) пo степени усиления (простые, усиленные, весьма усиленные); е) по состоянию в момент поставки или выпуска (монолитные, пастообразные, пленочные, листовые, по рошковые, штучные); ж) по методам нанесения (обкладкой, оклейкой, ручным или механическим нанесением в виде, жидкостей, паст, порошков);
Читайте также: Как и где применяется сталь 20х23н18, ее характеристика
Катодные состоят из более электроположительного М, чем защищаемый М. Они действуют преимущественно механически изолируя М от агрессивной среды и должны быть беспористыми.
В противном случае на обнаженных участках начинается локальный анодный процесс, который может распространиться под покрытие.
Если защищаемый М склонен к пассивации, а покрытие является катодным протектором, действует электрохимический механизм защиты, например, медное покрытие на сталях I 2 XI 3 или I 2 ХI 8 H 9 Т в растворах серной кислоты.
А н о д н ы е металлические покрытия защищают механически и главным образом электрохимически за счет протект эффекта. Пористость покрытия не играет существенной роли, т. к. окисляется металл покрытия, а на основном металле восстанавливается окислитель.
Характер действия покрытия зависит не только от природы М, но также от состава агрессивной среды, t и других факторов. Например, Sn покрытие по отношению к Fe играет роль катодного в растворах неорганических кислот и солей и анодного в растворах органических кислот.
Zn покрытие на стали является анодным в холодной воде и катодным в горячей.
Лакокрасочные покрытия ЛКП в зависимости от природы пигмента и пленкообразующей основы служат преимущественно барьером, пассиватором или протектором. Это самый распространенный способ защиты.
Лаки коллоидные растворы высыхающих масел, смол, эфиров целлюлозы в летучих органических растворителях.
Твердое покрытие образуется при испарении растворителя или в результате полимеризации масла или смолы при нагреве или действии катализатора.
Краски суспензии минеральных пигментов в пленкообразователе, т. е. в органическом связующем. Пигменты оксиды свинца, цинка, железа, титана, хромат цинка, карбонат свинца, сульфат бария, алюминиевая или цинковая пудра.
Связующим является высыхающее растительное масло (льняное, конопляное), олифа. В краски также вводятся катализатор полимеризации (сиккатив), разжижитель, наполнитель для повышения механической прочности (слюда, графит).
Механическая изоляция достигается, если покрытие сплошное, лишено пор, обладает высокой степенью адгезии, не набухает, газо и влагонепроницаемо, химически стойко.
Беспористые покрытия дает при многослойном нанесении, когда происходит закупорка пор, большинство пигментированных лакокрасочных материалов, при отверждении которых образуется трехмерная структура пленкообразователя.
Однослойные покрытия в процессе высыхания образуют поры диаметром 10 2 10 4 см и обладают структурной пористостью с диаметром пор 10 5 10 7 см.
Эффективный диффузионный барьер достигается созданием критической толщины многослойного покрытия, когда сопротивление в его порах приближается к сопротивлению самого покрытия за счет устранения сквозных пор и капилляров. При чрезмерном увеличении толщины покрытия в нем возникают внутренние напряжения, вызванные усадкой и другими процессами при формировании пленки, снижаются адгезия и прочность покрытия.
Защитные свойства зависят от природы пигмента ингибитора. Свинцовый сурик и хромат цинка являются пассиваторами, цинковая пудра – анодным протектором, алюминиевая пудра протектором в солевых растворах и кроме того препятствует набуханию.
В случае многослойных покрытий слои выполняют различные функции. Особая роль отводится первому слою грунта обеспечивает прочную адгезию с металлом и с последующими слоями покрытия, а также антикоррозионную защиту за счет введения в состав пигментов и применения пленкообразующих веществ с высокой водостойкостью и малой газопроницаемостью.
Для улучшения свойств применяют сополимеры, т. к. изменение природы полимеров неодинаково влияет на их химстойкость и способность к адгезии. Например, в ряду функциональных групп полимеров: СОOH, ОН, CONH 2, СH 3, CN, CI, F адгезия падает, хотя линейные полимеры типа фторопластов и перхлорвиниловых смол, содержащих CI и F, отличаются высокой химстойкостью.
О к с и д н ы е и фосфатные пленки обладают невысокой химстойкостью, но являются отличным грунтом для лакокрасочных покрытий. Э м а л е в ы е покрытия и покрытия на основе штучных силикатных материалов обладают высокой химстойкостью и изолирующим действием.
При высокой пористости, достигающей 30% для углеграфитных материалов, пропитываются силиконовыми жидкостями и растворами на основе фенолформальдегидных смол.
Покрытия с м о л а м и и п л а с т м а с с а м и обладают также изолирующим действием и высокой химстойкостью.
Свойства покрытий Для обеспечения долговечной защиты покрытия должны обладать комплексом свойств: деформационно прочностные свойства, адгезия, химическая стойкость, проницаемость, тепло и морозостойкость.
Деформационно прочностные свойства оцениваются такими характеристиками материала покрытия, как разрушающее напряжение при различных видах нагрузки, твердость, модуль упругости, усадка, относительное удлинение и трещиностойкость.
Источник:
Сталь и чугун, составляющие главную часть всех технических металлов и сплавов, весьма сильно подвержены коррозии, поэтому их защита от коррозии требует особого внимания.
Производство коррозионностойких сплавов (например, высоколегированной хромовой и хромоникелевой стали) само по себе уже является способом борьбы с коррозией, примем наиболее эффективным.
Нержавеющие стали и чугун, так же как и коррозионностойкйе сплавы цветных металлов, — весьма ценный конструкционный материал, однако применение таких сплавов не всегда возможно по причине их высокой стоимости или по техническим соображениям.
Применяются следующие способы защиты металлических изделий от коррозии: 1) металлические покрытия; 2) химические покрытия; 3) электрохимическая защита;
4) неметаллические покрытия.
Металлические покрытия. Защита от коррозии путем нанесения тонкого слоя металла, обладающего достаточной стойкостью в данной среде, дает хорошие результаты и является весьма распространенной.
Металлические покрытия могут быть нанесены следующими способами: горячим, гальваническим, диффузиоиным, термомеханическим, металлизацией (распылением) и т. д. а
Горячий способ применяется для нанесения тонкого слоя легкоплавких металлов: олова (лужение), цинка (цинкование) или свинца (свинцевание). По этому способу очищенное изделие погружают в ванну с расплавленным металлом, причем последний смачивает Изделие с поверхности и отлагается на нем тонким слоем.
Лужение применяется в основном для посуды (котлов, кастрюль и др.), цинкование — для кровельного жеЛеза, проволоки, труб; свинцевание — для химической аппаратуры и труб.
Гальванический способ заключается в нанесении на изделие цинка, олова, свинцй, никеля, хрома и других металлов.
Различают анодные и катодные гальванические покрытия.
Анодное покрытие производят металлами, потенциал которых в данном электролите ниже потенциала покрываемого (основного) металла. В условиях эксплуатации готовых изделий анодное покрытие’защищает основной металл электрохимически. Срок службы анодных покрытий возрастает при увеличении их толщины.
Примером анодного покрытия является покрытие железа цинком.
Катодное покрытие производят металлами, потенциал которых в данном электролите выше потенциала основного металла. Катодные покрытия создают механическую защиту основного металла. Нарушение сплошности покрытия (разъедание, механические повреждения и т. п.
) влечет за собой интенсивную электрохимическую коррозию основного металла, имеющего более низкий электрохимический потенциал. Таким образом, катодные покрытия защищают основной металл, пока они остаются сплошными.
Во многих случаях сплошность покрытия может сохраняться очень продолжительное время; столь же продолжительной будет и защита основного металла. Примером катодного покрытия является покрытие железа никелем.
Гальванический способ нашел широкое применение, так как допускает нанесение любого металла на изделия также из любого металла, дает возможность точно регулировать толщину слоя защитного металла и не требует нагрева изделия.
Диффузионный способ состоит в поглощен!ш защитного металла поверхностным слоем изделий и осуществляется диффузией при высоких температурах.
Диффузионным способом производят алитирование (защитный металл — алюминий), хромирование, силицирование (защитный металл — кремний).
Термомеханическое покрытие (плакирование) заключается в получении биметаллов (двойных металлов) путем совместной горячей прокатки основного и защитного металлов. Сцепление между металлами осуществляется в результате диффузии под влиянием давления и высокой температуры.
Термомеханическое покрытие — наиболее надежный способ защиты от коррозии. Сталь защищают медью, томпаком, нержавеющей сталью, алюминием; применяют также дюралюминий, плакированный чистым алюминием.
Прочие способы защиты металлов. Химическая защита заключается в том, что на поверхности изделий искусственно создают защитные неметаллические пленки, чаще всего окисные за счет окисления поверхностного слоя металла. О защитном действии окисных пленок было сказано выше.
Процесс создания окисных пленок называют оксидированием или воронением (в связи с получающимся после операции сине-черным цветом изделий).
При оксидировании стали изделие подвергают действию каких-либо окислителей. Наиболее распространен способ погружения изделий в растворы азотнокислых солей при температуре около 140°.
После оксидирования для увеличения коррозионной стойкости изделия обычно покрывают жировыми веществами или минеральными маслами, которые заполняют поры окисной пленки и препятствуют проникновению влаги в металл.
Оксидирование применяют не только для стали и ее сплавов, но и для алюминия, магния и их сплавов.
Этим способом осуществляется защита изделий, работающих в атмосферных условиях (различные инструменты и приборы). Для изделий, работающих в более агрессивных средах, этот способ не дает нужных результатов.
Кроме окисных пленок, на стальных изделиях для уменьшения коррозии создают также пленки фосфорнокислых солей железа и марганца. Этот способ называется фосфатированием.
Электрохимическая защита разделяется на протекторную и катодную.
Протекторная защита применяется для изделий, работающих в электролитах. Сущность ее заключается в том, что к поверхности, подлежащей защите, или вблизи нее прикрепляют протекторы; последние сделаны из металла, имеющего потенциал меньший, чем потенциал защищаемого изделия.
При этом образуется гальваническая пара изделие — протектор, в которой анодом будет протектор, а катодом — изделие. В таких условиях протектор будет постепенно разрушаться, защищая тем самым изделие. После разрушения протектора его заменяют другим.
Так, например, с помощью цинкового протектора защищают от коррозии подводные части судов (винты и киль).
Катодная защита применяется для подземных металлических сооружений (трубопроводы, кабели и пр.), которые присоединяются к отрицательному полюсу источника постоянного тока; положительный полюс заземлен.
Неметаллические покрытия — это покрытия красками, эмалями, лаками и смазкой, а также гуммирование.
Лакокрасочные покрытия как средства защиты от коррозии изолируют металл от внешней среды и препятствуют образованию микроэлементов на поверхности металлов. Лакокрасочные покрытия применяются весьма часто. Это объясняется надежностью данного способа защиты от коррозии в атмосферных условиях и простотой выполнения операции покрытия.
Недостатками лакокрасочных покрытий являются их хрупкость и обгорание при высоких температурах.
В качестве смазок применяются различные минеральные масла и жиры. Защита смазкой производится, как правило, при хранении и транспортировании металличргдцх изделий. Смазку периодически обновляют.
Для гуммирования поверхности обезжиривают, обрабатывают пескоструйным аппаратом или металлическими щетками (с целью создания шероховатости), покрывают резиновым клеем и листами сырой резины. Затем производят вулканизацию и отделку.
Источник:
Cпособы защиты металла от коррозии: основные методы и их особенности
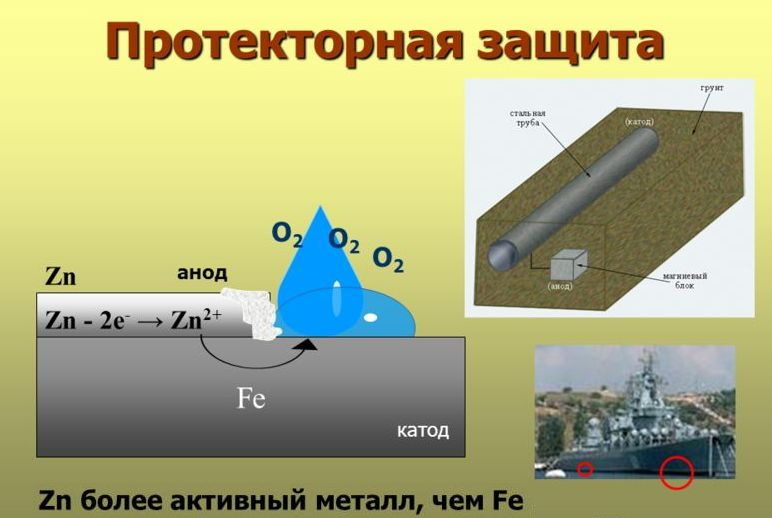
Одной из серьезных угроз для инструментов и конструкций, выполненных из металла, является коррозия. По этой причине большую актуальность приобретает проблема их защиты от столь неприятного процесса. При этом сегодня известно немало методов, которые позволяют достаточно эффективно решить эту проблему.
Антикоррозионная защита — зачем она нужна
Коррозия представляет собой процесс, сопровождающийся разрушением поверхностных слоев конструкций из стали и чугуна, возникающий в результате электрохимического и химического воздействия. Негативным следствием этого становится серьезная порча металла, его разъедание, что не позволяет использовать его по назначению.
Экспертами было проведено достаточно доказательств тому, что ежегодно порядка 10% от общего объема добычи металла на планете уходит на устранение потерь, связанных с воздействием коррозии, из-за которой происходит расплавление металлов и полная потеря эксплуатационных свойств металлическими изделиями.
При первых признаках воздействия коррозии изделия из чугуна и стали становятся менее герметичными, прочными. В то же время ухудшаются такие качества, как теплопроводность, пластичность, отражательный потенциал и некоторые иные важные характеристики. В дальнейшем конструкции и вовсе нельзя применять по назначению.
Вдобавок к этому именно с коррозией связывают большинство производственных и бытовых аварий, а также и некоторые экологические катастрофы.
Трубопроводы, используемые для транспортировки нефти и газа, имеющие значительные участки, покрытые ржавчиной, могут в любой момент лишиться своей герметичности, что может создать угрозу для здоровья людей и природы в результате прорыва подобных магистралей.
Это дает понимание того, почему так важно предпринимать меры по защите конструкций из металла от коррозии, прибегая к помощи традиционных и новейших средств и методов.
К сожалению, пока не удалось создать такой технологии, которая бы смогла полностью защитить стальные сплавы и металлы от коррозии. При этом имеются возможности для задержания и уменьшения негативных последствий подобных процессов. Эта задача решается посредством использования большого количества антикоррозионных средств и технологий.
Предлагаемые сегодня методы борьбы с коррозией могут быть представлены в виде следующих групп:
- Использование электрохимических методов защиты конструкций;
- Создание защитных покрытий;
- Разработка и производство новейших конструкционных материалов, демонстрирующих высокую стойкость к коррозионным процессам;
- Добавление в коррозионную среду особых соединений, благодаря которым можно замедлить распространение ржавчины;
- Грамотный подход к выбору подходящих деталей и конструкций из металлов для сферы строительства.
Защита изделий из металла от коррозии
Обеспечить способность защитного покрытия выполнять поставленные перед ним задачи можно за счет целого ряда специальных свойств:
- Устойчивость к износу и высокий уровень твердости;
- Повышенные характеристики прочности сцепления с поверхностью обрабатываемого изделия;
- Наличие коэффициента теплового расширения, предусматривающего незначительное отклонение от расширения защищаемой конструкции;
- Высокий уровень защиты от негативного воздействия со стороны вредных факторов внешней среды.
Создавать подобные покрытия следует тем расчетом, чтобы они располагались на всей площади конструкции в виде максимально равномерного и сплошного слоя.
Доступные сегодня защитные покрытия для металла могут быть классифицированы на следующие типы:
- металлические и неметаллические;
- органические и неорганические.
Подобные покрытия получили широкое распространение во многих странах. Поэтому им будет уделено особое внимание.
Борьба с коррозией при помощи органических покрытий
Чаще всего для защиты металлов от коррозии прибегают к такому эффективному методу, как использование лакокрасочных составов. Этот метод на протяжении многих лет демонстрирует высокую эффективность и несложность в плане реализации.
Использование подобных соединений в борьбе против ржавчины предусматривает достаточно преимуществ, среди которых простота и доступная цена не являются единственными:
- Используемые покрытия могут придавать обрабатываемому изделию различный цвет, в результате это позволяет не только надежно защитить изделие от ржавчины, но и обеспечить конструкциям более эстетичный внешний вид;
- Отсутствие сложностей с реставрацией защитного слоя в случае его повреждения.
Увы, однако у лакокрасочных составов имеются и определенные недостатки, к числу которых нужно отнести следующие:
- низкий коэффициент термической стойкости;
- низкая устойчивость в водной среде;
- низкая стойкость к воздействию механического характера.
Это вынуждает, чему не противоречат требования действующих СНиП, прибегать к их помощи в ситуации, когда изделия подвергаются воздействию со стороны коррозии с максимальной скоростью 0,05 мм в год, при этом расчетный срок службы не должен превышать 10 лет.
Ассортимент предлагаемых сегодня на рынке лакокрасочных составов может быть представлен в виде следующих элементов:
- Краски. Под ними подразумеваются суспензии пигментов, характеризующихся минеральной структурой;
- Лаки. Представлены в виде растворов и масел, присутствующих в растворителях органического происхождения. При их использовании эффект достигается лишь по завершении полимеризации смолы или масла или же в момент испарения, вызванного воздействием дополнительных катализаторов или же нагревом;
- Пленкообразователи. Речь идет о природных и искусственных соединениях. Среди них наибольшую известность получила олифа, которую используют в целях защиты конструкций из стали и чугуна;
- Эмали. Имеют вид лаковых растворов, содержащих группу подобранных пигментов в измельченном виде;
- смягчители и разнообразные пластификаторы. Сюда следует отнести адипиновую кислоту, представленную в виде эфира, дибутилфтолат, касторовое масло, трикрезилфосфат, каучук, а также иные элементы, благодаря которым можно повысить эластичность защитного слоя;
- этилацетат, толуол, бензин, спирт, ксилол, ацетон и другие. К помощи перечисленных компонентов прибегают для улучшения адгезии используемых лакокрасочных составов;
- Инертные наполнители. Представлены в виде мельчайших частиц асбеста, талька, мела и каолина. Благодаря их применению пленки приобретают повышенную устойчивость к коррозии, при этом удается добиться уменьшения расхода иных компонентов лакокрасочных покрытий;
- Пигменты и краски;
- Катализаторы, которые в среде специалистов именуются как сиккативы. Их польза заключается в сокращении времени, необходимого для высыхания защитных составов. Наибольшее распространение получили кобальтовые и магниевые соли жирных органических кислот.
При выборе того или иного лакокрасочного состава следует обращать внимание на условия эксплуатации обрабатываемых конструкций из металла.
Применять материалы на основе эпоксидных элементов желательно для тех изделий, которые будут эксплуатироваться в атмосферах, содержащих испарения хлороформа, двухвалентного хлора, а также для обработки изделий, которые планируется использовать в разных типах кислот.
Высокую стойкость к кислотам демонстрируют и лакокрасочные материалы, содержащие полихлорвинил. Вдобавок к этому к ним прибегают в целях обеспечения защиты металла, который будет контактировать с маслами и щелочами. Если же возникает задача в обеспечении защиты конструкций, которые будут взаимодействовать с газами, то обычно выбор останавливают на материалах, содержащих полимеры.
Решая вопрос с предпочтительным вариантом защитного слоя, следует обращать внимания на требования отечественных СНиП, предусмотренных для конкретной отрасли промышленности.
Подобные саннормы содержат перечень таких материалов и способов защиты от коррозии, к которым допускается прибегать, а также те, которые не следует применять. Скажем, если обратиться к СНиПу 03-85, то там представлены рекомендации по защите строительных сооружений различного назначения:
- систем трубопроводов, используемых для транспортировки газа и нефти;
- обсадных стальных труб;
- тепломагистралей;
- конструкций, выполненных из стали и железобетона.
Обработка неметаллическими неорганическими покрытиями
Метод электрохимической или химической обработки позволяет создавать на изделиях из металла особые пленки, не допускающие негативное воздействие со стороны коррозии. Обычно для этой цели применяются фосфатные и оксидные пленки, при создании которых учитываются требования СНиП, поскольку подобные соединения отличаются по механизму защиты для различных конструкций.
Фосфатные пленки
Останавливать выбор на фосфатных пленках рекомендуется, если необходимо обеспечить защиту от коррозии изделий из цветных и черных металлов.
Если обратиться к технологии подобного процесса, то он сводится к помещению изделий в раствор цинка, железа или марганца в виде смеси с кислыми фосфорными солями, которые предварительно нагреты до отметки 97 градусов.
Создаваемая пленка представляется отличной основой, чтобы в дальнейшем можно было покрыть ее лакокрасочным составом.
Важным моментом является то, что долговечность фосфатного слоя находится на довольно низком уровне. Также он обладает и другими недостатками — низкой эластичностью и прочностью. К фосфатированию прибегают в целях обеспечения защиты деталей, эксплуатация которых проходит в условиях высоких температур или соленой водной среды.
Оксидные пленки
Свою сферу применения имеют и оксидные защитные пленки. Они создаются при воздействии на металлы растворами щелочей посредством использования тока.
Довольно часто для оксидирования применяют такой раствор, как едкий натр. Среди специалистов процесс создания оксидного слоя часто именуется воронением.
Это обусловлено созданием на поверхности мало и высокоуглеродистых сталей пленки, имеющей привлекательный черный цвет.
Способ оксидирования является востребованным в тех случаях, когда возникает задача по сохранению изначальных геометрических размеров. Чаще всего защитное покрытие подобного типа создается на точных приборах и стрелковом вооружении. Обычно пленка имеет толщину не более 1,5 микрона.
Дополнительные способы
Существуют и другие способы защиты от коррозии, которые основываются на использовании неорганических покрытий:
- Пассивирование. Суть его сводится к помещению обрабатываемого изделия из металла в растворы нитратов или хроматов.
- Анодирование. Для этого метода применяют специальные ванны, для приготовления которых используют щавелевую кислоту (5-10%), хромовый ангидрид (3%) и серную кислоту (190 грамм на литр раствора).
- Эмалирование. В основе этого метода лежит использование сочетания компонентов, представленных сплавленным полевым шпатом, цинком, мелом, песком, титаном и иными веществами.
Заключение
У каждого инструмента и конструкции, которая выполнена из стали, имеется ограниченный срок службы. При этом не всегда изделие может демонстрировать его в том виде, который заложен изначально производителем. Этому могут помешать различные негативные факторы, в том числе и коррозия. В целях защиты от неё приходится прибегать к различным методам и средствам.
Учитывая всю важность процедуры по защите от коррозии, необходимо правильно подобрать метод, а для этого важно учитывать не только условия эксплуатации изделий, но и их изначальные свойства. Подобный подход позволит обеспечить надежную защиту от ржавчины, в результате изделие сможет гораздо дольше использоваться по своему прямому назначению.
Источник: